6月1日起,第三类医疗器械新法规强制来袭!如何从容应对?

▲自6月1号起第三类医疗器械(含体外诊断试剂)
要求应具有医疗器械唯一标识码(UDI)

2021年11月18日,国家药监局公开印发《关于做好第二批实施医疗器械唯一标识工作的公告》,自2022年6月1日起正式实行。
“
实施品种
在《国家药监局 国家卫生健康委 国家医保局关于深入推进试点做好第一批实施医疗器械唯一标识工作的公告》规定的9大类69个品种的基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围。支持和鼓励其他医疗器械品种实施唯一标识。
“
实施要求
纳入第二批实施唯一标识的医疗器械注册人应当按照以下要求开展工作:
(一)唯一标识赋码
2022年6月1日起,生产的医疗器械应当具有医疗器械唯一标识;此前已生产的第二批实施唯一标识的产品可不具有唯一标识。生产日期以医疗器械标签为准。
(二)唯一标识注册系统提交
2022年6月1日起,申请首次注册、延续注册或者注册变更时,注册申请人/注册人应当在注册管理系统中提交其最小销售单元的产品标识。
(三)唯一标识数据库提交
2022年6月1日起生产的医疗器械,在其上市销售前,注册人应当按照相关标准或者规范要求将最小销售单元、更高级别包装的产品标识和相关数据上传至医疗器械唯一标识数据库,确保数据真实、准确、完整、可追溯。
“
有关要求
医疗器械注册人要切实落实企业主体责任,鼓励基于唯一标识建立健全追溯体系,做好产品召回、追踪追溯等有关工作。
医疗器械经营企业要在经营活动中积极应用唯一标识,做好带码入库、出库,实现产品在流通环节可追溯。
医疗机构要在临床使用、支付收费、结算报销等临床实践中积极应用唯一标识,做好全程带码记录,实现产品在临床环节可追溯。

▲关于UDI
UDI 码是一个条形码,由数字、字母或者符号组成,附载在医疗器械产品或者包装上,用于对医疗器械进行唯一性识别。医疗器械唯一标识(UDI)包括产品DI和生产标识(PI),未来UDI码将印在医疗器械产品标签上。
简单来说“UDI”就是医疗器械产品的身份证,在出现医疗器械违规情况时,就可以通过UDI自动识别并精准追踪到所属企业,以此来倒逼生产企业在生产和销售过程中严格把控质量。


▲金蝶云·星空UDI一体化解决方案
基于金蝶云·星空强大的业务平台,将UDI融入到业务系统中,让医疗器械企业真正实现一体化的解决方案,减少异构系统之间的对接问题。
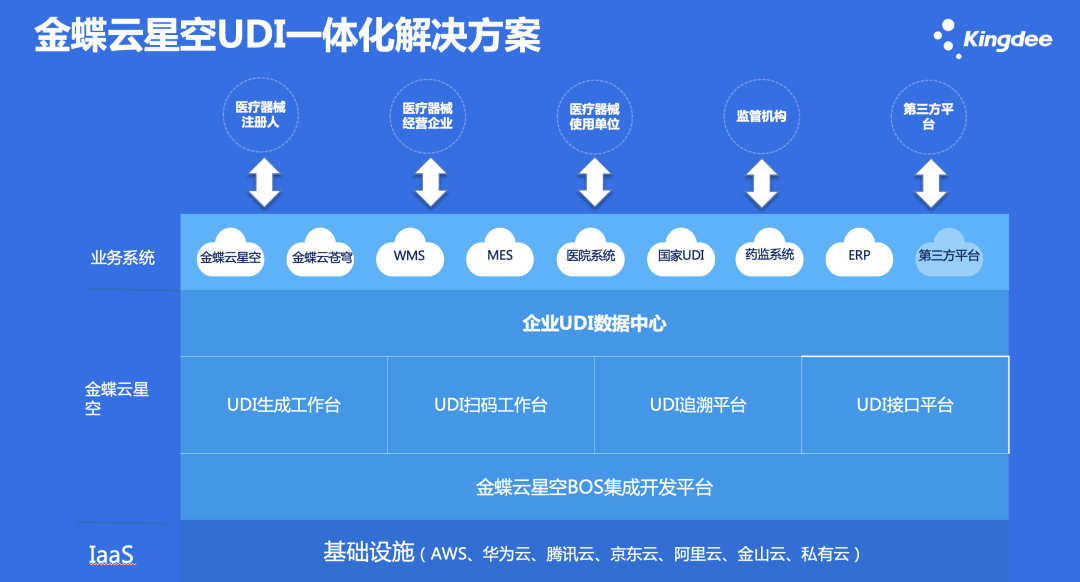
🔹 实现基于UDI在生产环节实现发码赋码及追溯工作
按照UDI试点要求,医疗器械注册人企业需要按照唯一标识系统规则和标准,对其产品创建和赋予唯一标识,完成唯一标识数据库数据上传工作,向下游企业或者使用单位提供唯一标识信息,探索建立唯一标识在产品追溯中的应用模式,形成相应的操作规范。
金蝶云·星空UDI解决方案不仅可以满足UDI的生成赋码工作及数据上传下载工作,同时将UD与ERP完全一体化融合,实现企业内部业务流程的协同一致性,既满足法规要求,同时也利用UDI来建立企业的质量追溯体系,提高内部生产及仓储的运作效率。
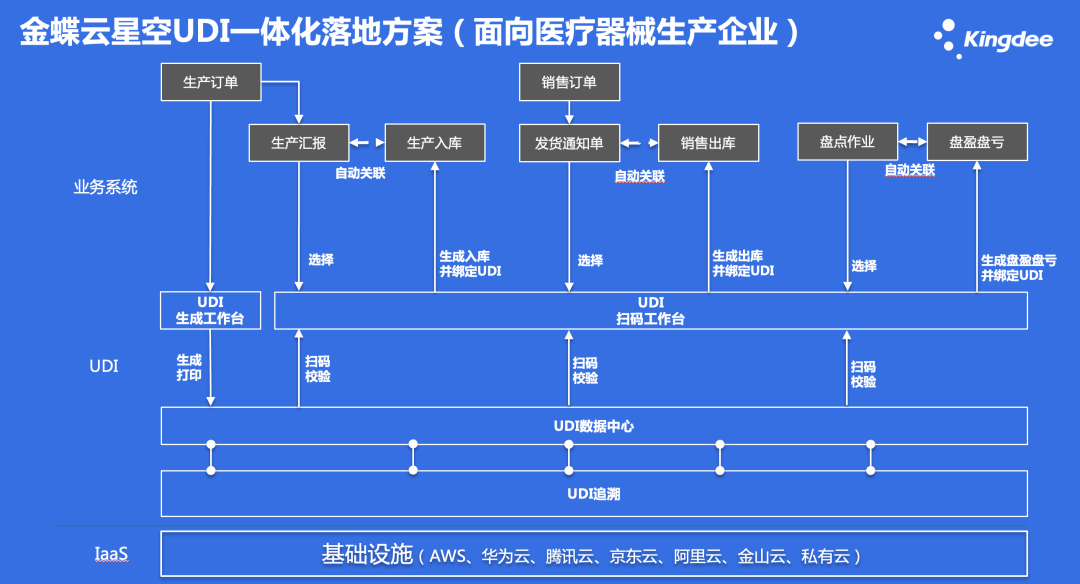
UDI发码赋码平台
为生产企业基于法规和企业管理需求制定合适的UDI编码规范,并为其导入编码规则,指导企业将UDI与现有标签系统相融合,协同生产企业进行生产线改造与软件升级,确立包装层级编码设计,实现在各级包装上应用合法的追溯识别标识码。
UDI追溯平台
协助生产企业将ERP流程与UDI相融合,在原材料、工序流程、库存、销售等环节实现全流程追溯,实现追溯可视化。使生产企业切实履行UDI赋码、追溯、召回、不良事件处理等义务。
🔹 基于UDI在经营流通环节实现追溯管理
按照UDI试点要求,医疗器械经营流通企业形成医疗器械经营流通业务中应用唯一标识的工作流程,验证多码并行的操作性,制定唯一标识数据库数据与业务系统的对接操作流程,探索与医疗器械注册人、使用单位、监管部门协同机制。
金蝶云·星空将UDI与GSP系统完全一体化融合,帮助经营流通企业制定在采购、验收、贮存、销售、运输、售后服务、不良事件报告、纠正、召回、投诉等供应链全过程业务环节追溯。
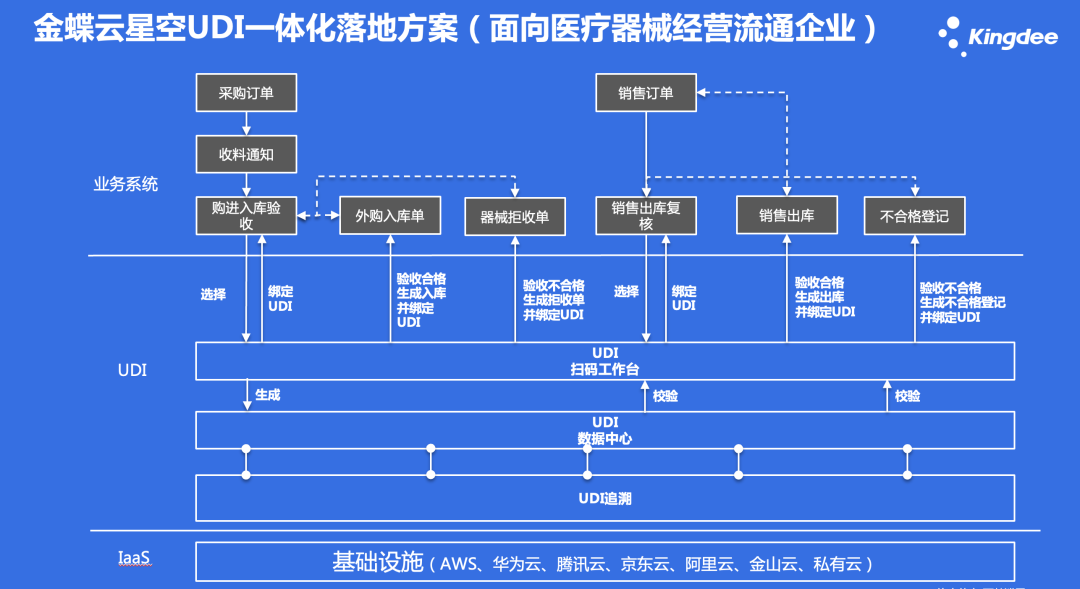
🔹 提供UDI 解析,使其可通过扫码录入UDI,实现质量的全程追溯跟踪:
✔可以在采购订单、采购收货、购进验收、销售订单、出库复核中,自动获取医疗器械UDI信息;
✔企业收货人员在接收医疗器械时,通过UDI 及UDI 数据库核实运输方式及产品是否符合要求;
✔实现扫 UDI 码即可对照相关采购记录与到货的医疗器械进行核对;加强对退货的管理,保证退货环节医疗器械的质量和安全,防止混入不合格医疗器械。

杭州智德专注为企业提供数字化一体解决方案
以“服务为王,价值共生”为战略宗旨
为企业不断发展提供系统化支撑,帮助客户成长
如需项目合作请扫描以下二维码咨询联系











